5.1 การกลั่นแบบธรรมดา (normal distillation) การกลั่นเป็นการแยกของเหลวที่สามารถระเหยได้ ซึ่งมีองค์ประกอบตั้งแต่ 2 ขึ้นไป การกลั่นแบบธรรมดาเหมาะสำหรับใช้กลั่นของผสมในของเหลวที่มี จุดเดือด (boiling point) แตกต่างกันมาก ๆ 5.2 การกลั่นลำดับส่วน (fractional distillation) การกลั่นลำดับส่วนเป็นวิธีการแยกของเหลวที่สามารถระเหยได้ตั้งแต่ 2 ชนิดขึ้นไป มีหลักการเช่นเดียวกันกับการกลั่นแบบธรรมดา คือเพื่อต้องการแยกองค์ประกอบในสารละลายให้ออกจากกัน แต่ก็จะมีส่วนที่แตกต่างจากการกลั่นแบบธรรมดา คือ การกลั่นแบบกลั่นลำดับส่วนเหมาะสำหรับใช้กลั่นของเหลวที่เป็นองค์ประกอบของสารละลายที่จุดเดือดต่างกันน้อยๆ ในขั้นตอนของกระบวนการกลั่นลำดับส่วน จะเป็นการนำไอของแต่ละส่วนไปควบแน่น แล้วนำไปกลั่นซ้ำและควบแน่นไอเรื่อย ๆ ซึ่งเทียบได้กับเป็นการการกลั่นแบบธรรมดาหลาย ๆ ครั้งนั่นเอง ความแตกต่างของการกลั่นลำดับส่วนกับการกลั่นแบบธรรมดา จะอยู่ที่คอลัมน์ โดยคอลัมน์ของการกลั่นลำดับส่วนจะมีลักษณะเป็นชั้นซับซ้อน เป็นชั้นๆ ในขณะที่คอลัมน์แบบธรรมดาจะเป็นคอลัมน์ธรรมดา ไม่มีความซับซ้อนของคอลัมน์ ชุดอุปกรณ์การกลั่นลำดับส่วน นอกจากนี้ ในการกลั่นแบบลำดับส่วน จะต้องมีการเพิ่มอุณหภูมิอย่างช้า ๆ ดังนั้น จำเป็นที่จะต้องมีอุปกรณ์ที่ให้ความร้อน (heater) และสามารถควบคุมอุณหภูมิได้ เพราะของผสมที่กลั่นแบบลำดับส่วนมักจะมีจุดเดือดที่ใกล้เคียงกัน ซึ่งตรงกันข้ามกับการกลั่นแบบธรรมดา ความร้อนที่ให้ไม่จำเป็นต้องควบคุมเหมือนการกลั่นลำดับส่วน แต่ก็ไม่ควรให้ความร้อนที่สูงเกินไป เพราะความร้อนที่สูงเกินไป อาจจะไปทำลายสารที่เราต้องการกลั่น เพราะฉะนั้น ประสิทธิภาพในการกลั่นลำดับส่วนจึงดีกว่าการกลั่นแบบธรรมดา 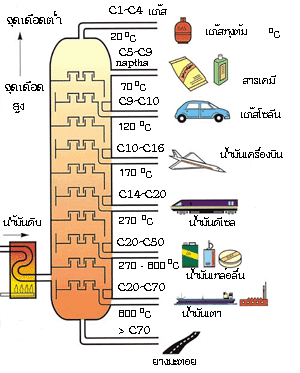 กระบวนการกลั่นลำดับส่วนที่นำมาใช้ในอุตสาหกรรมปิโตรเลียม ตัวอย่างการนำการกลั่นลำดับส่วนมาใช้ประโยชน์ เช่น การแยกของผสมระหว่างเบนซีน (benzene) กับโทลูอีน (toluene)
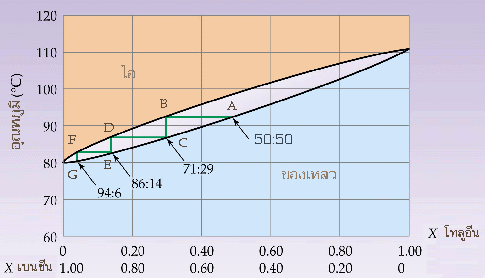
ปกติ เบนซีน กับ โทลูอีน เป็นสารที่ไม่มีสีทั้งคู่ แต่ที่นักเรียนมองเห็นเป็นสีเทา (เบนซีน) และสีน้ำตาล (โทลูอีน) ในขวดรูปกรวย ก็เพื่อต้องการให้นักเรียนพิจารณาปริมาณสารที่อยู่ในขวดชมพู่ควบคู่กับอัตราส่วนของเบนซีนที่แยกออกจากโทลูอีนในกราฟ ค่า X เป็นเศษส่วนโมล จากกราฟจะเห็นได้ว่า จุดเดือดของโทลูอีน (toluene) สูงกว่าเบนซีน (benzene) แสดงว่าความดันไอของโทลูอีน จะต่ำกว่าเบนซีน ถ้านำของผสมที่จุด A ซึ่งมีอัตราส่วนของเบนซีนต่อโทลูอีนเป็น 50: 50 มาให้ความร้อนจนกลายเป็นไอ ซึ่งของผสมจะเดือดที่ จุด B องค์ประกอบของไอที่จุด B จะมีอัตราส่วนของเบนซีนต่อโทลูอีนเป็น 71: 29 และถ้านำไอที่จุด B มาควบแน่นจะได้ของเหลวผสมที่จุด C แล้วให้ความร้อนจนกลายเป็นไอ ของเหลวผสมจะเดือดที่ จุด D องค์ประกอบของไอที่จุด D จะมีอัตราส่วนของเบนซีนต่อโทลูอีนเป็น 86 : 14 จะเห็นได้ว่าองค์ประกอบของเบนซีนที่อยู่ในไอเพิ่มมากขึ้น ถ้าทำซ้ำเช่นนี้ไปเรื่อย ๆ จะสามารถแยกเบนซีนออกมาเป็นไอบริสุทธิ์ได้ ส่วนของเหลวที่เหลือจะเป็นโทลูอีนที่บริสุทธิ์ เพราะฉะนั้น การกลั่นลำดับส่วนของสารละลายที่สมบูรณ์แบบ จะสามารถแยกองค์ประกอบของเหลวออกจากกันได้อย่างบริสุทธิ์ | ||||||||||||||
คลังบทความ
30 ส.ค. 2554
การกลั่น
สมัครสมาชิก:
ส่งความคิดเห็น (Atom)
จำนวนการดูหน้าเว็บรวม
คลังความรู้ต่างๆ
ยินดีต้อนรับผู้ที่เข้ามาเยี่ยมชมทั้งหลายครับ
ไม่มีความคิดเห็น:
แสดงความคิดเห็น